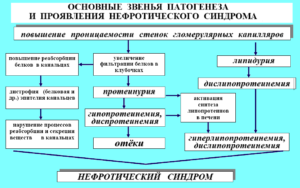
Патогенез отеков при нефротическом синдроме
Содержание
Нефротический синдром

Нефротический синдром характеризуется главным образом протеинурией, которая может быть клубочковой, канальцевой и гиперпротеинемической.
- Клубочковая протеинурия развивается при повышении проницаемости клубочкового фильтра для белков.
- Канальцевая – при нарушении реабсорбции белков в проксимальных канальцах.
- Гиперпротеинемическая – при избытке белка в крови (легких цепей иммуноглобулинов).
Этиология, патогенез, патологическая анатомия
Нефротический синдром развивается только при клубочковой протеинурии. Основными заболеваниями, приводящими к нефротическому синдрому, являются:
- болезнь минимальных изменений,
- фокально-сегментарный гломерулосклероз,
- мембранозная нефропатия,
- мезангиокапиллярный гломерулонефрит,
- диабетический гломерулосклероз,
- амилоидоз.
Болезнь минимальных изменений
Болезнь минимальных изменений, или липоидный нефроз, развивается при дисбалансе между субпопуляциями Т-лимфоцитов.
В большинстве случаев болезнь возникает без видимых причин (идиопатический вариант), реже – при системных заболеваниях (лимфогрануломатозе, сахарном диабете, ВИЧ-инфекции, IgA-нефропатии, болезни Фабри) и применении лекарств (НПВС, рифампицина, интерферона α, комплекса декстран-железо).
Морфологические изменения выявляют только при электронной микроскопии. Обнаруживают отек с диффузным набуханием отростков эпителиальных подоцитов, вакуоли, лизомы и увеличенное число органелл.
Фокально-сегментарный гломерулосклероз
Первичный фокально-сегментарный гломерулосклероз характеризуется склерозом и гиалинозом отдельных петель клубочка (отсюда сегментарный) менее чем в половине клубочков (фокальный), в большинстве случаев бывает идиопатическим, реже развивается при ВИЧ-инфекции, героинизме, лизосомных болезнях накопления.
Вторичный фокально-сегментарный гломерулосклероз развивается после гибели части почечной паренхимы, приводящей к повышению внутриклубочкового давления, при врожденной агенезии почки; после резекции почки при туболоинтерстициальном нефрите, серповидной анемии.
При гистологическом исследовании обнаруживают слияние ножек подоцитов и сегментарный склероз клубочков, узелковые и крупнозернистые отложения IgМ и СЗ.
Мембранозная нефропатия
Мембранозная нефропатия характеризуется диффузным утолщением базальных мембран клубочковых капилляров. Причины первичной мембранозной нефропатии неизвестны.
Вторичная осложняет течение системных заболеваний (злокачественных новообразований, СКВ, гепатита В) или развивается при введении пеницилламина и препаратов золота. При электронной микроскопии на ранних стадиях болезни выявляют субэпителиальные отложения с выступами lamina densa между ними.
Позже отложения образуются внутри ГБМ, происходит диффузное и гранулярное распределение IgG вдоль нее без клубочковой пролиферации, экссудации и некроза.
Мезангиокапиллярный гломерулонефрит
Мезангиокапиллярный гломерулонефрит бывает двух типов, сходных по основным морфологическим признакам (увеличение числа клеток в мезангии, расширение мезангиального матрикса, двухконтурность и утолщение базальных мембран, дольчатость клубочков) и различающихся по локализации и составу отложений.
При I типе отложения субэндотелиальные и мезангиальные, они содержат СЗ, IgG или IgМ. При II типе отложения содержат СЗ, не содержат иммуноглобулинов и располагаются внутри мембран.
Мезангиокапиллярный гломерулонефрит – иммунокомплексное заболевание, которое развивается при инфекционном эндокардите, ВИЧ-инфекции, гепатитах В и С, СКВ и злокачесвенных новообразованиях (лейкозах и лимфоме).
Симптомы
Основным признаком нефротического синдрома является протеинурия обычно больше 2 г/м2. Протеинурия обусловлена повышением проницаемости клубочкового фильтра при повреждении клубочковой базальной мембраны и фильтрационных щелей между ножками подоцитов.
Следствием протеинурии является гипоальбуминемия, уровень которой зависит от количества выводимого с мочой альбумина. Гипоальбуминемия обусловлена также распадом реабсорбированного альбумина в проксимальных канальцах и нарушением синтеза альбумина в печени.
Ведущим клиническим признаком заболевания являются отеки, возникающие исподволь, постепенно нарастающие и достигающие нередко степени анасарки с асцитом, гидротораксом и гидроперикардом.Но первичное обращение к врачу может быть связано с очаговым отеком из-за жалоб на затрудненное дыхание (отек гортани или плевральный выпот), загрудинную боль (гидроперикард), распухшие колени (гидроартроз), боли в животе (отек брыжейки), набухание мошонки.
https://www.youtube.com/watch?v=KFpUKWPUtzA
Отеки обычно появляются по утрам на веках и лице и в коленях ближе к вечеру после хождения. По мере прогрессирования заболевания отеки становятся постоянными и массивными, приводящими к растяжению кожи с образованием бледных атрофических участков – стрий, особенно на животе и бедрах. Патогенез отеков сложен.
Жидкость скапливается главным образом в связи с гипоальбуминемией и изменением соотношения гидравлического и онкотического давления в капиллярах и интерстиции (старлинговые силы) и повышением канальцевой реабсорбции Na и воды, обусловленным усиленной секрецией АДГ и активацией ренин-ангиотензинальдостеронового механизма.
Еще один важный диагностический признак данного синдрома – гиперлипопротеидемия. Уровни ЛПНП и холестерина повышены у большинства больных, а ЛПОНП и триглицеридов – в наиболее тяжелых случаях. Но риск атеросклероза и ИБС при нефротическом синдроме не доказан.
При нефротическом синдроме обычно развиваются нарушения свертывания крови за счет уменьшения активности антикоагулянтных и фибринолитических факторов сывороточных протеиназ.
Нарушения свертываемости крови и эпизодическая гиповолемия создают риск ТЭЛА, тромбоза периферических сосудов, особенно почечных вен.
Характерными клиническими симптомами являются недомогание, анорексия, увеличение массы тела, атрофия мышц, которая может быть замаскирована отеком. В зависимости от степени выработки у больных ангиотензина II возможны гипо-, нормо- или гипертензивное состояние.
Осложнения
Осложнения развиваются при длительно существующем нефротическом синдроме. К ним относятся:
- дефицит питательных веществ, включая белковую недостаточность, проявляющуюся ломкостью волос и ногтей, задержкой роста, деминерализацией костей;
- синдром недостаточности калия;
- миопатия;
- снижение метаболизма.
В связи с потерей иммуноглобулинов нередко развиваются инфекционные заболевания. Артериальная гипертензия может осложниться поражением сердца и головного мозга. Но возможно развитие ортостатической гипотензии и гиповолемического шока, иногда с фатальным исходом.
Диагностика
Анализ мочи выявляет значительную протеинурию с экскрецией 3,5 г и более белка в сутки. В мочевом осадке выявляют обычно гиалиновые, восковидные, зернистые и эпителиальноклеточные цилиндры. Протеинурия при гломерулонефрите может сочетаться с гематурией и лейкоцитурией.
В крови снижается содержание альбумина (меньше 1,5–2,5 г%), уровней α- и γ-глобулинов, адренокортикальных и тиреоидных гормонов, а также трансферина, антистрептолизина-О, других Ig и комплемента.
Наоборот, при системной красной волчанке уровень IgG повышен, при очаговом гломерулосклерозе – снижен, при мембранозном гломерулонефрите уровень СЗ нормальный.
азота мочевины и креатинина в сыворотке крови зависит от степени поражения почек.
Нарушение свертываемости крови обусловлено выведением IX, XII и тромболитических факторов (урокиназы и антитромбина III) с мочой и повышением содержания фактора VIII, фибриногена и тромбоцитов в сыворотке.Потеря с мочой трансферрина приводит к развитию микроцитарной анемии. Для нефротического синдрома характерно увеличение в сыворотке общего холестерина, триглицеридов, свободного и эстерифицированного холестерина и фосфатов.
Резко повышенная концентрация липидов сочетается с выраженной гипоальбуминемией.
Диагноз основывается на клинических проявлениях и лабораторных исследованиях. Однако окончательный диагноз ставится только после гистологического и электронно-микроскопического исследования биоптатов почки.
Дифференциальный диагноз:
- В первую очередь проводится между первичным нефротическим синдромом, для которого характерны тяжелая протеинурия, выраженные биохимические изменения сыворотки и сравнительно позднее развитие почечной недостаточности, и вторичным нефротическим синдромом, при котором почечная недостаточность имеется уже к началу нефротического синдрома или развивается вскоре после этого.
- Болезнь минимальных изменений встречается чаще у детей и характеризуется гипертензией и азотемией.
- Мембранозно-пролиферативный гломерулонефрит также развивается главным образом у детей (60–80% случаев), протекает с макрогематурией, азотемией и артериальной гипертензией.
- Мезангиокапиллярный гломерулонефрит выявляется чаще у взрослых больных (75%), протекает с микрогематурией в 20% и гипертензией в 35% случаев.
Течение и прогноз
Течение нефротического синдрома длительное, прогноз зависит от этиологии. Более благополучный прогноз при заболеваниях, поддающихся лечению кортикостероидами.
Некоторые из них, например мезангиокапиллярный гломерулонефрит, могут проходить самостоятельно через 5–8 лет. При болезни минимальных изменений прогноз у 90% детей и взрослых хороший.
Рецидивы у них возникают часто, но поддаются лечению, и почечная недостаточность обычно не развивается.
Мембранозная нефропатия протекает медленно, постепенно прогрессирует до почечной недостаточности у 50% больных на протяжении 15–20 лет, у 50% могут сохраняться протеинурия или нефротический синдром без нарушения функции почек.
Тяжелее протекают фокально-сегментарный гломерулосклероз и мезангиокапиллярный гломерулонефрит, при которых почти у половины больных развивается хроническая почечная недостаточность в течение 8–10 лет. Лечение кортикостероидами обычно не эффективно.
Стойкая ремиссия наблюдается у немногих больных (5%).
После трансплантации почек рецидивы нефротического синдрома часто развиваются у больных с фокально-сегментарным гломерулосклерозом, мезангиокапиллярным гломерулонефритом, СКВ, Ig – нефропатией.
Прогноз обычно ухудшается при инфекционных заболеваниях, азотемии, артериальной гипертензии, выраженной азотемии, тромбозах периферических сосудов.
Лечение
Лечение больных проводится с учетом нозологической формы, вызвавшей нефротический синдром, функционального состояния почек, продолжительности и особенностей его течения. Не следует строго ограничивать режим и диету больных.
Больным назначают лечебную физкультуру, ежедневную ходьбу до 3–4 км, полноценное питание с содержанием животного белка в пище до 1 г/кг массы тела и снижение потребления натрия хлорида до 5 г/сут. Медикаментозное лечение включает: лечение основного заболевания, снижение протеинурии и уменьшение отдельных клинических проявлений.
Лечение основного заболевания
При болезни минимальных изменений рекомендуют первичную терапию преднизолоном в дозе 1–1,5 мг/кг внутрь в течение 4–6 нед. Положительный эффект проявляется прекращением протеинурии и увеличением диуреза.
В последующем больные переводятся на поддерживающую терапию преднизолоном по 2–3 мг/кг через день в течение 4 нед и затем дозу постепенно в течение последующих 4 мес сводят на нет.
Если больные не реагируют на кортикостероиды или развиваются частые рецидивы, рекомендуется назначение преднизолона с циклофосфамидом по 2–3 мг/кг/сут в течение 3 нед или хлорамбуцилом по 0,2 мг/кг/сут в течение 12 нед.
Такое лечение обычно эффективно, но цитостатические препараты вызывают многочисленные побочные эффекты (подавление функции половых желез, иммунитета, цистит, канцерогенность), особенно в препубертатном возрасте. Возможно назначение вместо алкилирующих средств циклоспорина внутрь по 5 мг/кг/сут в два приема. Циклоспорин вызывает ремиссию в 60–80% случаев, но после уменьшения дозы возможен рецидив.Нефротический синдром при мембранозной нефропатии проходит без лечения у 40%, у 35–40% он протекает волнообразно – с рецидивами и ремиссиями, у остальных 20–25% он сохраняется постоянно, при этом постепенно нарушается функция почек, и через 10–15 лет развивается терминальная почечная недостаточность. Эффективность глюкокортикоидов, циклофосфамида, хлорамбуцила и циклоспорина не доказана. При терминальной хронической почечной недостаточности показана трансплантация почки.
Лечение фокально-сегментарного гломерулосклероза не эффективно. Протеинурия может быть уменьшена 8-недельным курсом преднизолона и циклофосфамида.
Восстановление клубочковой фильтрации и снижение протеинурии возможно при лечении циклоспорином в дозах, применяемых при лечении болезни минимальных изменений. Ремиссия обычно непродолжительная, быстро развивается рецидив.
Не существует доказательств эффективности лечения нефротического синдрома антикоагулянтами и антитромболитическими средствами.
При мезангиокапиллярном гломерулонефрите эффективно лечение глюкокортикоидами в сверхвысоких дозах (“пульс-терапия”), чередующимися с хлорамбуцилом.
Преднизолон назначают по 1000 мг в/в в течение 3 дней, а затем внутрь по 0,4 мг/кг/сут в течение 27 дней; хлорамбуцил – внутрь по 0,2 мг/кг/сут. Курс лечения 6 мес.
Возможно назначение антиагрегантов (дипиридамола 200–400 мг/сут и аспирина 300–500 мг/сут).
Снижение протеинурии и уменьшение клинических проявлений
В комплекс лечения включают ингибиторы АПФ, которые могут снижать протеинурию и липемию. Но при тяжелой почечной дисфункции они могут усилить гиперкалиемию.
При массивных отеках и асците целесообразно проводить лечение тиазидовыми диуретиками. Но они могут привести к гипокалиемии и метаболическому алкалозу. Поэтому при их назначении следует дополнительно использовать препараты калия. Кроме того, диуретики в больших дозах уменьшают объем плазмы, что может привести к ухудшению функции почек и угрозе тромбоза.
При выраженной гиповолемии, угрожающей развитием гиповолемического шока, необходимы вливания плазмы или альбумина. Артериальную гипертензию лечат диуретиками, ингибиторами АПФ и антагонистами кальция. Бактериурия, эндокардит, перитонит и другие очаги инфекции требуют своевременного выявления и интенсивного лечения.
НПВС уменьшают протеинурию, вероятно, за счет снижения кровотока в клубочках, но они не влияют на активность процесса. Учитывая способность этих препаратов вызывать острую почечную недостаточность, задержку натрия и воды, гиперкалиемию и другие побочные эффекты, их применяют ограничено.
Источник: http://medicoterapia.ru/nefroticheskiy-sindrom.html
Нефрит и отеки

Заболевания почек влияют как на мочевыделительную систему, так и на организм в целом.
Примером этого являются нефротические отеки, возникающие при болезни почек различного генеза, проявляющиеся сначала на лице, а потом на всем теле.
Причина развития этого состояния лежит в нарушении обмена веществ, что ведет к искажению баланса белков и жиров, которые относятся к главным составным стенки сосудов.
Что называют отечным нефротическим синдромом?
Заболевания воспалительного, аутоиммунного, травматического генеза проявляются нарушениями одного из основных процессов в почках: фильтрации, реабсорбции и секреции. Нефротический синдром — это совокупность симптомов, возникающих на фоне значительной потери протеинов с мочой, нарушении белкового и жирового обмена, что проявляется отеками и повышением артериального давления.
Условия возникновения
Причины развития нефротического синдрома:
- разные виды нефрита — воспаление почек;
- системная красная волчанка;
- амилоидоз почек — отложение крахмала;
- сахарный диабет;
- нефрит у беременных;
- геморрагическая форма васкулита — воспаление микрососудов;
- аллергические состояния;
- токсическое поражение почек;
- онкологические заболевания.
Патогенез возникновения отеков
Механизм нефротических отеков связан с нарушением проницаемости клубочков нефронов для белков. Повышенная проницаемость ведет к тому, что альбумины и глобулины проходят через почечный барьер и выводятся с мочой. Таким образом, количество этих показателей в крови значительно уменьшается. Потеря белков провоцирует понижение онкотического давления, регулируемого уровня протеинов.
При такой патологии белок выводится с мочой, а вода с натрием задерживается в виде отеков.
Падение давления, в свою очередь, проявляется выходом жидкости из сосудов, и уменьшением объема циркулирующей крови, что выражается развитием отеков.
Снижение объема крови является критическим состоянием для организма, поэтому активируется симпатическая нервная и ренин-ангиотензиновая системы.
В ответ на это возникает задержка ионов Na и воды, что повышает уровень проявления в отечном синдроме.Патогенез повышения артериального давления основан на том, что снижение объема циркулирующей крови ведет к рефлекторному сокращению мышц стенки сосудов и активации централизации кровообращения. А также стимуляция работы симпатической нервной системы с выбросом адреналина и норадреналина способствуют повышению давления.
Как проводится диагностика нефротических отеков?
Отеки при нефритах исследуют с помощью лабораторных методов:
- Общий анализ крови — при воспалении почек возможны изменения лейкоцитов в сторону их увеличения, нейтрофильный сдвиг лейкоцитарной формулы влево, повышение СОЭ.
- Биохимическое исследование венозной крови — уменьшение общего количества белков ниже 50 г/л, снижение показателя альбуминов — 30 г/л и ниже, нарушение соотношения между альбуминами и глобулинами. Показатели холестерина, липопротеинов низкой и очень низкой плотности, триглицеридов выше нормы.
- Общий анализ мочи — количество белка выше 3,5 г в анализе, что соответствует потерей протеинов 30—45 г/сутки, наличие воскообразных цилиндров, слизи, жировых включений. При нефрите острого течения в моче имеются лейкоциты, эритроциты и бактерии.
Дальше болезнь усугубляется, проявляясь отечностью тела и высоким артетриальным давлением.
Для подтверждения, что отеки возникли через нарушение работы почек, нужно собрать детальный анамнез и провести первичный осмотр.
В выяснении жалоб нужно обратить внимание на то, выражен ли отечный синдром на лице с утра, уменьшается ли до второй половины дня или становится почти незаметным.
Дальнейшее развитие болезни характеризуется отечностью всего тела на фоне повышения артериального давления.
При осмотре отеков нужно обратить внимание на их симметричность, структуру и цвет. Это важно, поскольку отеки при нефротическом синдроме за этими характеристиками отличаются от таких при заболеваниях сердечно-сосудистой системы. Эти манипуляции не занимают много времени и помогают определить источник отечности.
Как лечить?
Помощь при нефротическом синдроме зависит от заболевания, которое его вызвало. На фоне основной терапии необходимо корректировать режим питья и употребление кухонной соли. Жидкость нужно принимать часто и небольшим количеством, а суточный объем должен быть умеренным. На период лечения лучше всего отказаться от употребления соли или свести ее количества к минимуму.
С целью выведения воды, которая накопилась в межклеточном пространстве и спровоцировала нефротическую отечность, применяют диуретики «Фуросемид» и «Гипотиазид» — типичные представители этой группы, успешно борющиеся с отечным синдромом. Они провоцируют выведение ионов калия, поэтому параллельно нужно принимать «Аспаркам» или «Панангин», которые приводят этот показатель в норму.
Хорошим дополнением будет применение растительных сборов, улучшающих функции почек. К ним относится чай из брусники, толокнянки и специальные комплексные почечные сборы.
Если уменьшение отеков не повлияло на артериальное давление, консервативную терапию дополняют гипотензивными препаратами, способными возвратить нормальный уровень давления. С этой целью применяют «Пропранолол», «Капроприл», «Верапамил». Важно, что лечение должно проходить под контролем врача, ведь борьбу с отеками можно начинать только тогда, когда известен источник их появления.
Источник: http://ProUrinu.ru/priznaki/vazhno/nefroticheskie-oteki.html
Отеки при нефротическом синдроме
Нефротический синдром может развиваться на фоне широкого круга урологических, системных, инфекционных, хронических нагноительных, метаболических заболеваний. В урологии нефротический синдром осложняет течение заболеваний почек примерно в 20% случаев.
Патология чаще развивается у взрослых (30-40 лет), реже у детей и пожилых пациентов. При нефротическом синдроме наблюдается классическая тетрада признаков: протеинурия (свыше 3,5 г/сут.), гипоальбуминемия и гипопротеинемия (менее 60-50 г/л), гиперлипидемия (холестерин более 6,5 ммоль/л), отеки.
В случае отсутствия 1-2-х проявлений говорят о неполном (редуцированном) нефротическом синдроме.
Причины развития нефротического синдрома
По происхождению нефротический синдром может быть первичным (осложняющим самостоятельные заболевания почек) или вторичным (следствием заболеваний, протекающих с вторичным вовлечением почек).
Первичный нефротический синдром встречается при гломерулонефрите, пиелонефрите, первичном амилоидозе, нефропатии беременных, опухолях почек (гипернефроме) и др.
Развитие вторичного нефротического синдрома может быть обусловлено многочисленными состояниями: коллагенозами и ревматическими поражениями (СКВ, узелковым периартериитом, геморрагическим васкулитом, склеродермией, ревматизмом, ревматоидным артритом); нагноительными процессами (бронхоэктазами, абсцессами легких, септическим эндокардитом); болезнями лимфатической системы (лимфомой, лимфогранулематозом); инфекционными и паразитарными заболеваниями (туберкулезом, малярией, сифилисом) и пр. В ряде случаев нефротический синдром развивается на фоне лекарственной болезни, тяжелых аллергозов, отравлений тяжелыми металлами (ртутью, свинцом), укусов пчел и змей и т. д.
Иногда, преимущественно у детей, причину нефротического синдрома выявить не удается, что позволяет выделить идиопатический вариант заболевания.
Среди концепций патогенеза нефротического синдрома наиболее распространенной и обоснованной является иммунологическая теория, в пользу которой свидетельствует высокая частота возникновения синдрома при аллергических и аутоиммунных заболеваниях и хороший отклик на иммуносупрессивную терапию. При этом образующиеся в крови циркулирующие иммунные комплексы являются результатом взаимодействия антител с внутренними (ДНК, криоглобулинами, денатурированными нуклеопротеидами, белками) или внешними (вирусными, бактериальными, пищевыми, медикаментозными) антигенами. Иногда антитела образуются непосредственно к базальной мембране почечных клубочков. Осаждение иммунных комплексов в ткани почек вызывает воспалительную реакцию, нарушение микроциркуляции в клубочковых капиллярах, развитие повышенной внутрисосудистой коагуляции.
Изменение проницаемости клубочкового фильтра при нефротическом синдроме ведет к нарушению абсорбции белка и его попаданию в мочу (протеинурия). Ввиду массивной потери белка в крови развивается гипопротеинемия, гипоальбуминемия и тесно связанная с нарушением белкового обмена гиперлипидемия (повышение холестерина, триглицеридов и фосфолипидов).
Развитие отеков при нефротическом синдроме обусловлено гипоальбуминемией, снижением осмотического давления, гиповолемией, уменьшением ренального кровотока, усиленной продукцией альдостерона и ренина, реабсорбцией натрия.
Макроскопически почки при нефротическом синдроме имеют увеличенные размеры, гладкую и ровную поверхность. Корковый слой на разрезе бледно-серый, а мозговой – красноватый.
Микроскопическое изучение тканевой картины почки позволяет увидеть изменения, характеризующие не только нефротический синдром, но и ведущую патологию (амилоидоз, гломерулонефрит, коллагенозы, туберкулез и т. д.).Собственно нефротический синдром в гистологическом плане характеризуется нарушениями структуры подоцитов (клеток капсулы клубочков) и базальных мембран капилляров.
Симптомы нефротического синдрома
Признаки нефротического синдрома однотипны, несмотря на различие вызывающих его причин.
Ведущим проявлением служит протеинурия, достигающая 3,5-5 и более г/сутки, причем до 90% выводимого с мочой белка составляют альбумины.
Массивная потеря белка с мочой вызывает снижение уровня общего сывороточного белка до 60-40 и менее г/л.
Задержка жидкости при нефротическом синдроме может проявляться периферическими отеками, асцитом, анасаркой (генерализованным отеком подкожной клетчатки), гидротораксом, гидроперикардом.
Прогрессирование нефротического синдрома сопровождается общей слабостью, сухостью во рту, жаждой, потерей аппетита, головной болью, тяжестью в пояснице, рвотой, вздутием живота, поносом. Характерным признаком нефротического синдрома служит олигурия с суточным диурезом менее 1 л.
Возможны явления парестезии, миалгия, судороги. Развитие гидроторакса и гидроперикарда вызывает одышку при движении и в покое. Периферические отеки сковывают двигательную активность больного. Пациенты с нефротическим синдромом вялые, малоподвижные, бледные; отмечают повышенное шелушение и сухость кожи, ломкость волос и ногтей.
Нефротический синдром может развиваться постепенно или бурно; сопровождаться менее и более выраженной симптоматикой, что зависит от характера течения основного заболевания.
По клиническому течению различаются 2 варианта нефротического синдрома – чистый и смешанный.В первом случае нефротический синдром протекает без гематурии и гипертензии; во втором может принимать нефротически-гематурическую или нефротически-гипертоническую форму.
Осложнениями нефротического синдрома могут явиться периферические флеботромбозы, вирусные, бактериальные, грибковые инфекции, отек мозга или сетчатки, нефротический криз (гиповолемический шок).
Диагностика нефротического синдрома
Ведущими критериями распознавания нефротического синдрома служат клинико-лабораторные данные.
При нефротическом синдроме объективный осмотр выявляет бледные («перламутровые»), холодные и сухие на ощупь кожные покровы, обложенность языка, увеличение размеров живота, гепатомегалию, отеки.
При гидроперикарде отмечается расширение границ сердца и приглушение тонов; при гидротораксе – укорочение перкуторного звука, ослабленное дыхание, застойные мелкопузырчатые хрипы.
На ЭКГ регистрируется брадикардия, признаки дистрофии миокарда.
В общем анализе мочи при нефротическом синдроме определяется повышенная относительная плотность (1030-1040), лейкоцитурия, цилиндрурия, наличие в осадке кристаллов холестерина и капель нейтрального жира, редко – микрогематурия.
В периферической крови – увеличение СОЭ (до 60-80 мм/ч), преходящая эозинофилия, увеличение числа тромбоцитов (до 500-600 тыс.), небольшое снижение уровня гемоглобина и эритроцитов. Нарушение свертываемости, выявляемые с помощью исследования коагулограммы, могут выражаться в небольшом повышении или развитии признаков ДВС-синдрома.
Источник: https://zdorovo.live/pochki/oteki-pri-nefroticheskom-sindrome.html
Что такое отечный нефротический синдром?
Нефротический отек, отечный синдром — одно из проявлений недуга при воспалении почек. Ему присуща значительная протеинурия, гипопротеинемия, а также гиперхолестеринемия (скачок холестерина в крови).
Уровень альбуминов при этом заболевании снижается. При этом кровоток почек остается неизменным. Натрий и вода всасываются значительно больше, отсюда наступает уменьшение диуреза. Повышается давление в венах.
Воспаление почек, как и другие болезни, дают нефротический синдром. Для установления диагноза и для получения прогнозов по болезни необходимо делать биопсию почек.
Опасность при отеках — жидкость из них просачивается через трещины в коже, что провоцирует сильное обезвоживание. Сегодня врачи способны не допустить сохранение долгосрочной отечности у пациентов.Благодаря тому, что медицина движется вперед, пациенты не так часто страдают нефротическими кризами (боли в животе, жидкий стул, рвота)
Причины синдрома и патогенез
Сахарный диабет может стать причиной синдрома.
Возможны разновидности нефротического синдрома, который дает воспаление почек. Клиническая картина и механизм нефротических отеков, а также патогенез может отличаться.
Вариативны и течение с морфологическими изменениями в почках. Основная причина нефротического синдрома — гломерулонефрит (хроническая форма заболевания и подострая), а также другие виды нефрита.
В остальных случаях этот нефритический отек дают:
- сахарный диабет;
- амилоидоз (дистрофия внутренних органов на фоне нарушения белкового обмена);
- плохое кровообращение в почках, которое является следствием повышенного давления в венах почки;
- тромбоз в венах парного органа.
Кроме того, нефротический синдром может сопровождать красную волчанку, нефропатию при беременности, плазмоцитому, сифилис, констриктивный перикардит, некоторые отравления. Отечность в первую очередь появляется на лице, а также на ногах, в области половых органов, на пояснице, на передней брюшной стенке. Она может смещаться, если сменить положение тела на длительное время.
Отек при воспалении почек может начаться из-за задержки натрия и усиленного выделения вазопрессина, также он может стать последствием онкотического давления (для распределения воды между лимфой и кровью) в плазме крови. Появление нефротического отека может быть местным, когда баланс жидкости нарушается. Если отек общий, то нарушается водный баланс в организме.
Диагностика нефротических синдрома
Необходимо определить уровень белка в моче для диагностики болезни.
С мочей человек, не имеющий воспаление почек, а с ним и нефротический синдром, выделяет белок в количестве 200 мг за день.
При нефротическом синдроме, когда есть воспаление почек и отеки при нефритах, его количество увеличивается до 20 г в день, реже — выше. В разные дни количество белка может колебаться.
Существует два вида проявления синдрома:
- В первом случает количество белка больше всасывающей способности нефрона.
- Во втором случае почка не дает проходить нормальным белкам, а патогенные белки пропускает.
Необходимо определить, какое первичное заболевание привело к появлению нефротического синдрома и его патогенез. Диагностически выясняют, где был локализирован первый отек (на лице, конечностях), при каких условиях появился, в каком положении тела. Был ли симптом вызван аллергией, заболеваниями сердца или других органов, есть ли одышка (или была), употребляется ли алкоголь.
Лечение синдрома
Заболевание будет успешно ликвидировано при правильном лечении основного недуга, который дал отек. В случаях, когда он обширный, пациенту нужно соблюдать постельный режим. Обязательна диета, при которой вводится ограничение на соленую пищу. При нефритах следует ограничить потребления жидкости.
При остром течении гломерулонефрита диета назначается строже, но не такая длительная. Такое ограничение в соли и воде при длительном применении может вызвать нарушение обмена веществ, а позже вероятно наступление азотемии и солевое истощение. При ограничении на употреблении воды пациенту нужно получать дополнительное количество белка.
В случаях протекания болезни с кахектическими отеками (при недостаточном поступлении пищи в организм) должны назначаться витамины B1, C, P.
Для лечения синдрома с отеками при нефрите необходимо применения лекарств, выводящих жидкость из организма. Диуретики выписывают индивидуально, рассчитав дозу.
Необходим постоянный контроль диуреза при лечении, нужно следить за весом пациента. Диуретики назначают в комбинации другими медикаментами — этакриновая кислота, «Хлорталидон», «Клопамид».
Эти препараты не должны вызывать потерю калия.
Лечение проводится также препаратами, сберегающими калий, так как диуретики способны вымывать этот элемент из организма. В диету вводятся продукты, богатые этим микроэлементов, иногда назначают препараты солей калия.
Если у пациента цирроз печени, то при недостатке этого элемента может возникнуть печеночная энцефалопатия.
В случаях, когда у пациента снижается коллоидно-осмотическое давление, возможно введение таких препаратов, как «Альбумина» или «Полиглюкин».
Источник: https://etopochki.ru/nefrit/info/nefroticheskie-oteki.html
Патогенез отеков при нефротическом синдроме – Все про почки
Многие годы пытаетесь вылечить ПОЧКИ?
Глава Института нефрологии: «Вы будете поражены, насколько просто можно вылечить почки просто принимая каждый день…
Читать далее »
Среди почечных патологий гломерулонефрит занимает не последнее место. Заболевание может протекать в хронической или острой форме. Хроническим гломерулонефритом принято называть иммунное воспалительное заболевание клубочкового аппарата почек, которое прогрессирует с каждым днем.
Болезнь может привести к развитию почечной недостаточности. Гемодиализ или трансплантация органа могут стать неизбежными последствиями заболевания. При отсутствии лечения гломерулонефрит хронический может развиваться дальше и вести к серьезным патологиям и летальному исходу.
Этиология почечной патологии
Хронический гломерулонефрит развивается по причинам, среди которых следующие:
НАШИ ЧИТАТЕЛИ РЕКОМЕНДУЮТ!
Для лечения почек наши читатели успешно используют Ренон Дуо. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
- наличие в организме очагов хронических инфекций (гайморит, холецистит, пародонтит);
- обнаружение нефритогенных штаммов стрептококка;
- персистирующие вирусные инфекции (грипп, гепатит, ветряная оспа, краснуха);
- наследственная предрасположенность (объясняется нарушениями на уровне клеточного иммунитета);
- лекарственная или алкогольная интоксикация, вакцинация;
- разнообразные иммуновоспалительные заболевания (васкулит, волчанка);
- почечные дисплазии.
Вышеперечисленные причины заболевания являются основными, но есть и второстепенные. Хронический гломерулонефрит поражает почки из-за переохлаждения организма и снижения сопротивляемости на фоне инфекционных заболеваний.
Патогенез болезни протекает следующим образом: клетки воспалительного инфильтрата выделяют медиаторы, которые приводят к образованию цитокинов. Последние оказывают разрушающее воздействие на структуру почечных клубочков, что постепенно и приводит к их склерозированию, а также развитию заболеваний других внутренних органов. Хронический гломерулонефрит может быть опасен не только для почек.
В течении заболевания выделяют фазы ремиссии и обострения. От медленно прогрессирующего нефрита человек может страдать около 7-10 лет.
Формы и симптомы хронического гломерулонефрита
В медицине выделяют следующие формы болезни:
- латентная;
- гипертоническая;
- гематурическая;
- нефротическая;
- смешанная.
Симптоматика по-разному проявляется в зависимости от вида хронического гломерулонефрита.
Если у пациента диагностировали латентный гломерулонефрит, признаки заболевания не являются четко выраженными. Сначала немного повышается артериальное давление.
Для этой формы характерен изолированный мочевой синдром без отечности. Для указанной патологии характерно постепенно прогрессирующее течение.
Пациент может оставаться трудоспособным, но при этом находиться под постоянным врачебным наблюдением.Гипертоническая или гипертензионная форма характеризуется не только сильным повышением давления, но и сердечной астмой, а также гипертрофией левого желудочка. Отечность так же, как и в первом случае, проявляется слабо. Эта патология наблюдается только у 20% пациентов и протекает достаточно пассивно. Диагностировать хронический гломерулонефрит из-за отсутствия отеков удается не сразу.
Больные с нефротическим синдромом страдают от выраженной протеинурии, понижения диуреза и значительного повышения плотности мочи.
Тахикардия, развитие плеврита, неуемная жажда и характерные отеки – вот основные симптомы нефротической формы гломерулонефрита.
В 30% случаев болезнь начинает протекать стремительно и может привести к серьезным последствиям, вплоть до недостаточности функционирования органа.
Хронический гломерулонефрит в гематурической форме встречается довольно редко – всего в 10% случаев от общего числа заболеваний.
Постоянная гематурия, макрогематурия и анемия – основные признаки подобной болезни. Отечность практически не наблюдается.
Согласно сведениям из медицинской практики, эта форма нефрита протекает благоприятнее остальных и редко ведет к почечной недостаточности и серьезным патологиям.Гипертоническая и нефротическая формы могут протекать с самыми опасными для человека последствиями. Но встречается еще смешанная разновидность гломерулонефрита, то есть одновременное проявление признаков вышеуказанных заболеваний. Правда, она выявляется лишь в 5% случаев. Отличается прогрессивным и быстрым течением. Неизбежно приводит к почечной недостаточности.
Диагностика хронического гломерулонефрита
Для получения точной клинической картины заболевания проводят необходимые диагностические исследования. Выводы делаются на основе полученных результатов анализов.
Общий анализ мочи – это главный метод для выявления симптомов почечного воспалительного процесса. Выявляется число лейкоцитов, эритроцитов, белка, определяется изменение удельного веса и плотность мочи.
Для того чтобы оценить работоспособность почек, берут специальные пробы Реберга и Зимницкого.
Затем потребуется общий анализ крови. При хроническом гломерулонефрите диагностируется содержание в кровяных тельцах антигиалуронидазы и антистрептокиназы. Их повышенное содержание говорит о развитии гиперхолестеринемии и диспротеинемии.
Если хронический гломерулонефрит протекает слишком активно, проводят ультразвуковое исследование почек, чтобы четко определить степень разрушения органа. При склерозировании почечной ткани происходит уменьшение размеров органа, что обязательно выявляется при помощи УЗИ. Для определения степени почечной дисфункции применяются такие методы, как пиелография, урография, нефросцинтиграфия.
Нередко в амбулаторных условиях медицинские специалисты отправляют пациентов на электрокардиограмму и УЗИ плевральных полостей. Эти методики позволяют выявить характер протекания болезни (с осложнениями или без).
Немаловажную роль играет и дифференциальная диагностика, благодаря которой можно отличить хронический гломерулонефрит от аналогичных по симптоматике заболеваний. Для этого проводят биопсию почки.
С помощью этого метода можно выявить форму болезни и определить, на какой стадии она находится.
Лечение и профилактика хронического гломерулонефрита
Указанное заболевание поддается лечению, особенно при первом обнаружении симптомов. После проведения диагностики пациенту назначается лечение для избавления от отеков и снижения артериального давления, а также предотвращения развития острой почечной недостаточности.
Больному обязательно потребуется соблюдать особый клинический режим и ограничивать себя в приеме некоторых блюд. Медицинские специалисты назначают еще и медикаментозное лечение при хроническом заболевании.
Правильный режим зависит от клинических проявлений гломерулонефрита. Кому-то необходимо избегать чрезмерных физических и психических нагрузок, переохлаждения организма. Предусмотрен обязательный двухчасовой дневной отдых. При проявлении простудных симптомов больному в обязательном порядке назначается общий анализ мочи. При резком ухудшении самочувствия его потребуется госпитализировать.
Диета обычно зависит от формы хронического гломерулонефрита. При изолированном мочевом синдроме рекомендуется снизить потребление поваренной соли до 10-15 г в сутки. Не следует злоупотреблять наваристыми мясными бульонами, а лучше от них отказаться.При гипертоническом и нефротическом синдромах норма потребления соли в сутки не должна превышать 6 г. Если же отечность все равно будет проявляться, потребуется снижение нормы до 4 г. Что касается содержания белка в пище, то рекомендованная доза – не более 1 г на 1 кг массы тела пациента.
За содержанием белка необходимо следить уже при первых проявлениях опасного заболевания. А вот прием жидкости должен быть увеличен до 2 л в сутки.
Медикаментозная терапия включает в себя:
- прием препаратов, подавляющих иммунное воспаление (глюкокортикостероиды);
- противовоспалительные средства;
- препараты для улучшения микроциркуляции в почках (курантил, фенилин).
Лекарственные средства помогают значительно отсрочить возникновение почечной недостаточности. Но их прием должен быть постоянным. Дозировка и конкретное расписание приема составляются врачом. Нельзя самостоятельно использовать те или иные препараты без назначения.
Если больной находился в стационаре, его могут выписать при улучшении состояния и наблюдать за ним амбулаторно. Амбулаторное наблюдение предполагает отслеживание функциональности почек пациента путем сдачи анализов. Важно рациональное лечение простудных заболеваний под медицинским присмотром.
При выраженной протеинурии и изолированном мочевом синдроме рекомендуется больше времени проводить на климатических курортах в Крыму, Ашхабаде, Бухаре.
Там располагаются специальные санатории для лечения больных хроническим гломерулонефритом. Правда, жаркий климат не показан при повышенном артериальном давлении и серьезных проявлениях симптомов недостаточности.
Общая длительность санитарно-курортного лечения не должна превышать 1,5 месяца в год.
Профилактика заболевания имеет особую важность, так как позволяет снизить опасность нарушения функции почек.
С этой целью больной должен несколько раз в год посещать гастроэнтеролога, кардиолога, уролога, ревматолога, стоматолога и других врачей. Не помешает рациональное закаливание, применение специальных сывороток и вакцин.
Но дополнительные лекарственные средства не могут быть использованы без консультации с медицинским специалистом. Важно, что серьезная болезнь поддается лечению.Источник: https://1pochki-med.ru/narodnye-sredstva/patogenez-otekov-pri-nefroticheskom-sindrome/